副猪嗜血杆菌病是由副猪嗜血杆菌( Haemophilus parasuis,Hps)引起猪的以多发性浆膜炎和关节炎为主要特征的猪的呼吸道传染病。该病常见于5~8周龄的猪,发病率一般在10%~15%,严重时病死率可达50%。主要引起猪纤维素性多发性浆膜炎和关节炎,急性型可引起败血症,在不出现典型的浆膜炎时就呈现发绀,皮下水肿和肺水肿,乃至死亡,急性感染后可能留下后遗症,如公猪跛行[1] [2]。近年来由于该病的频发,给养猪业带来了严重的经济损失,该病有效的防制措施是进行疫苗免疫。按Kieletein -Rapp-Gabriedson (KRG)血清分型方法,目前HPs至少可分为15个血清型[3],其中多数菌株可引起仔猪发病,部分菌株为条件性致病菌。不同血清型副猪嗜血杆菌之间的交叉保护力具有可变性。Rapp-Gabrielson 等研究了副猪嗜血杆菌血清2、4、5、12、13和14型菌株间的交叉保护性,结果表明血清型4能保护同源菌株和血清5型HPs攻击,而血清型5型菌株只能保护同源菌株攻毒,血清4、5型的二价菌苗能显著降低血清13型和血清12型攻击造成的病变程度和死亡率[4]。
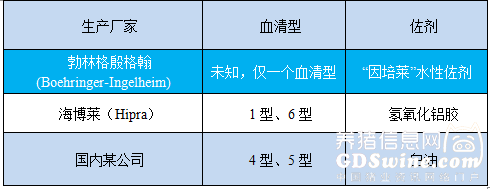
在我国,副猪嗜血杆菌在各猪场引起多发性浆膜炎和关节炎的报道屡见不鲜,从北京、黑龙江、辽宁、河南、湖南、宁夏、湖北等省市分离出副猪嗜血杆菌4型、5型和13型[5]。对于副猪嗜血杆菌市场疫苗来说,菌株上包含 1到2个血清型,所使用的佐剂有水性佐剂、铝胶佐剂或白油佐剂(见表1),目前的主要问题包括:制苗用菌株血清型与国内流行株血清型不符、油佐剂灭活疫苗免疫猪后有残留及副反应。
表1 国内副猪嗜血杆菌病灭活疫苗产品信息
1、副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株)优势特点
普莱柯生物工程股份有限公司、洛阳惠中生物技术有限公司、国家兽用药品工程技术研究中心联合开发了副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株),大量实验室研究表明本产品安全、无副反应,免疫仔猪或免疫怀孕母猪后所产哺乳期仔猪攻毒保护率均在80%以上;该疫苗应用于规模化猪场进行临床实验,结果表明猪场副猪嗜血杆菌病的发病率显著下降。另外,采用高效进口水性佐剂和高效全自动超滤生产工艺技术,使该疫苗具有注射方便、易吸收、无残留、无副反应、对胴体品质无任何影响等特点。
1.1 毒株 疫苗毒株精心筛选自国内优势血清型,可有效预防和控制我国猪场流行的副猪嗜血杆菌病。
1.2 进口水性佐剂灭活疫苗 在国家高新技术研究发展计划(863计划)重大专项支持下,研发过程中筛选出能增强免疫效果、安全性高的水溶性佐剂,在保证免疫效果的前提下提高了疫苗的安全性。
1.3 生产工艺先进 采用高效生物发酵技术和全自动进口超滤浓缩设备,生产工艺先进,产品质量稳定。
1.4 免疫期为6个月,且对12型、13型副猪嗜血杆菌菌株表现不同程度的交叉保护,。
1.5 减少抗生素使用,提高饲料转化率,降低死淘率。
2、副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株)实验室研究
2.1 免疫佐剂的筛选
为了使制备的副猪嗜血杆菌病二价灭活疫苗具备安全性好,无毒副作用,并能取得满意免疫效果,我们分别用水溶性佐剂、氢氧化铝佐剂、水包油佐剂、白油佐剂制备疫苗A、B、C、D,从安全性和免疫效力方面进行佐剂筛选试验(见表2、3),最终筛选出水溶性佐剂用于生产制备副猪嗜血杆菌病二价灭活疫苗。
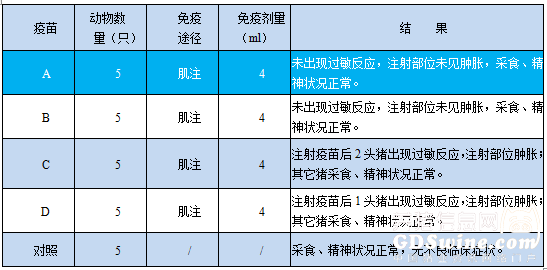
表2 不同佐剂副猪嗜血杆菌病灭活疫苗对仔猪的安全性
注:过敏反应症状:呕吐、精神沉郁、站立不稳; “/”表示此项无内容。
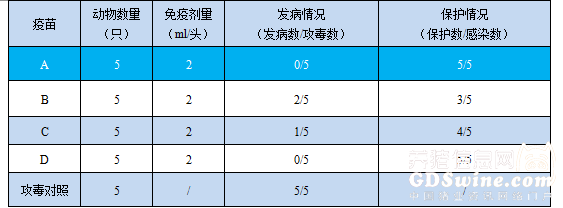
表3 不同佐剂副猪嗜血杆菌病灭活苗仔猪免疫攻毒保护试验结果
2.2 发酵及超滤工艺研究
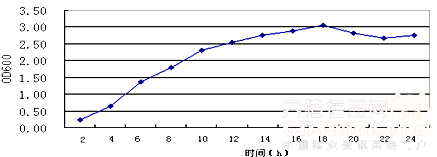
采用高密度生物发酵技术和独特的培养基配方,将菌液浓度(OD600值)由2.5提高到3.05,活菌数升高了1倍,提高了有效抗原含量(见图1);采用高效全自动进口超滤生产工艺技术,减少内毒素、去除异源蛋白,抗原更纯净。
图1 副猪嗜血杆菌高密度发酵生长曲线
2.3 疫苗的安全性研究
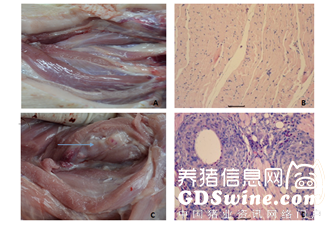
为了研究疫苗的安全性,我们用研制的水性佐剂灭活疫苗和油佐剂对照疫苗进行比较试验,从疫苗外观、显微镜下观察(见图2),到颈部肌肉注射疫苗4ml/头,观察猪精神状况、采食、饮水情况,同时观察注射部位是否产生炎性肿胀等临床不良反应,试验观察期结束时随机抽取仔猪剖检,观察注射部位疫苗吸收情况,并进行组织病理学检查(见图3)。结果油佐剂灭活疫苗为乳剂、黏度大,注射后易造成注射部位局部肿胀等炎性反应,免疫猪后有残留且有一定的应激副反应;水性佐剂灭活疫苗为混悬液、分散均匀,注射方便快捷,吸收好,无副反应。

图2.不同佐剂疫苗外观和显微镜观察结果对比
图3 左侧为注射部位剖检观察结果对比,右侧为组织病理学观察(HE染色,放大倍数均为200倍,比例尺均为50μm)结果对比
A:水性佐剂疫苗注射后14日,注射部位疫苗吸收完全,其它均未见异常;
B:水性佐剂疫苗注射后14日,注射部位肌肉组织学观察,注射部位仅见少量淋巴细胞浸润,其它均未见异常;
C:油佐剂对照疫苗注射后14日,注射部位见少量未吸收疫苗、肉芽肿(箭头所示);
D: 油佐剂对照疫苗注射后14日,注射部位肌肉组织学观察,注射部位见少量未吸收疫苗,见成纤维细胞、巨噬细胞、
2.4 疫苗的效力研究
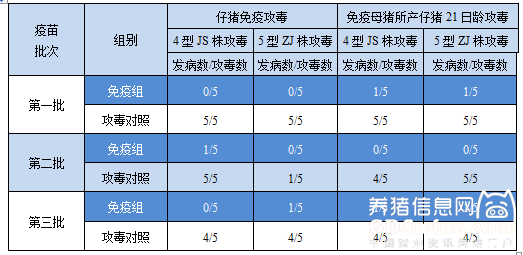
三批疫苗分别免疫仔猪和怀孕母猪,仔猪在3~4周龄首免,3周后二免,怀孕母猪在产前8~9周首免,3周后二免;仔猪二免后14日各组随机抽取10头和未免疫对照仔猪10头,于本公司动物房负压区内进行攻毒保护试验;免疫怀孕母猪和未免疫怀孕母猪所产断奶前仔猪各10头于公司动物房负压区内进行攻毒保护试验;每组分别用一个发病剂量的副猪嗜血杆菌4型JS株和5型ZJ株攻毒,结果免疫组攻毒保护率均在80%(4/5)以上,对照组的发病率均在80%(4/5)以上,攻毒保护结果见表4。
表4 仔猪免疫攻毒试验和仔猪被动免疫攻毒试验结果
3、副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株)田间试验
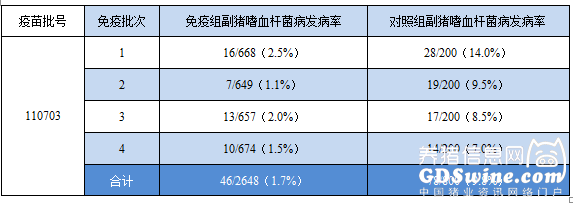
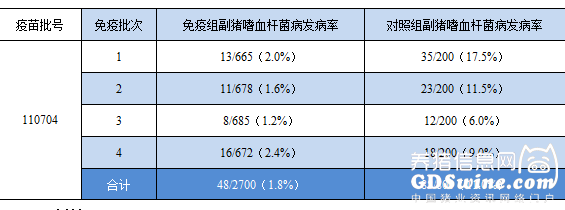
郑州某猪场(猪场规模:母猪4000头)和洛阳某猪场(猪场规模:母猪2000头)对副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株)进行应用。免疫的疫苗批号分别为110703和110704,规格为100ml/瓶,品种分别为杜-长-大和大-长-大三元杂交猪。每个猪场分4批次免疫,每批选取650头左右3周龄健康仔猪,采用颈部肌肉注射疫苗,免疫剂量为2ml。首次免疫后3周加强免疫,免疫剂量和免疫方式与首免相同。每个猪场另外每批选取200头3周龄健康仔猪作对照组,不免疫副猪嗜血杆菌病二价灭活疫苗。免疫组和对照组的饲养管理与其他疫苗的预防免疫按常规方法进行,饲养至24周龄出栏,期间观察并统计各猪场的副猪嗜血杆菌病的发病率。结果表明郑州某猪场使用疫苗加强免疫后,副猪嗜血杆菌病的发病率显著下降,由9.8%下降至1.7%,免疫组比对照组发病率降低了8.1%;洛阳某猪场使用疫苗加强免疫后,副猪嗜血杆菌病的发病率也显著下降,由11.0%下降至1.8%,免疫组比对照组发病率降低了9.2%,具体结果见表5、表6。
表5 郑州某猪场免疫副猪嗜血杆菌病二价灭活疫苗效果
表6 洛阳某猪场免疫副猪嗜血杆菌病二价灭活疫苗效果
4、讨论
实验室研究结果表明,副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株)安全性良好,不仅对仔猪有较好免疫效果,且免疫母猪其子代具有母源抗体保护,说明该疫苗免疫母猪也有较好免疫效果。疫苗应用于规模化猪场,田间试验数据表明猪场副猪嗜血杆菌病的发病率显著下降,免疫组比对照组发病率降低8.1%以上,且免疫猪群的副猪嗜血杆菌病的发病率均控制在2.5%以下,同时也表明猪场发生的副猪嗜血杆菌病主要是由4型、5型副猪嗜血杆菌引起。综上所述,副猪嗜血杆菌病二价灭活疫苗(4型JS株+5型ZJ株)可以有效保护规模猪场猪只不受副猪嗜血杆菌感染,减少猪场经济损失,值得推广应用。
参考文献
[1] Oliveiar S, Pijoan C. Haemophilus parasuis: new ternds on diagnosis, epidemiology and contorl[J] . Veterinary Microbiology, 2004, 99: L-12.
[2] Oliveira S, Galina L, Blanco I, et al. Naturally-farrowed, artificially-reared pigs as an alternative model for experimental infection by Haemophilus parasuis [J]. Can J Vet Res. 2003, 67(2):146-150.
[3] Rafiee M, Blackall P.J. Establishment, validation and use of the Kielstein-Rapp-Gabrielson Serotyping scheme for Haemophilus parasuis. Australian Vetrinary Journal,2000,78(3):172-174.
[4] Rapp-Gabrielson VJ, Gabrielson DA. Prevalence of Haemophilus parasuis serovars among solates from swine[J]. Am J Vet Res, 1992, 53(5): 659-664.
[5] 蔡旭旺. 副猪嗜血杆菌的分离鉴定及诊断方法与灭活疫苗的研究[D]. 华中农业大学博士论文, 2006.
(来源:国家兽用药品工程技术研究中心 作者: 王生富 廖永洪 胡东波 白晶晶 谷世江)
| 查看所有评论 最新评论 |
|
|
| 发表评论 | ||||
|